Многие газы в физике принято описывать в рамках идеальной модели, с помощью которой можно легко определить основные термодинамические характеристики системы. В данной статье приведем вывод формулы Майера для газа идеального и покажем, как ее можно использовать для решения задачи.
Идеальный газ и его уравнение
Чтобы понять вывод формулы Майера, следует ближе познакомиться с моделью идеального газа. Согласно ей, термодинамическая система представляет собой совокупность частиц, которые не обладают размерами (являются материальными точками). Их кинетическая энергия является единственной компонентой внутренней энергии системы (потенциальная энергия взаимодействий равна нулю), и скорости частиц подчиняются классическому распределению Максвелла-Больцмана.
 Вам будет интересно:Что такое полати. Примеры пословиц
Вам будет интересно:Что такое полати. Примеры пословиц
Описанная модель хорошо подходит для многих реальных газообразных систем, состоящих из химически инертных атомов и молекул, и имеющих невысокие давления и температуры в несколько сотен кельвин.
Идеальный газ описывается универсальным выражением, которое называется законом Клапейрона-Менделеева. Оно приведено ниже:
P*V = n*R*T.
Здесь P, V, T - три термодинамических величины: давление, объем и температура. Параметры n и R - это количество вещества в системе и постоянная для всех газов, соответственно.
Внутренняя энергия и изохорный процесс
Согласно определению, внутренняя энергия U произвольной системы равна сумме потенциальной и кинетической энергий ее элементов. Выше отмечалось, что в идеальной модели газовые молекулы и атомы друг с другом не взаимодействуют, это означает, что внутренняя энергия определяется исключительно кинетической составляющей.
Из кинетической теории газов следует равенство, связывающее среднюю кинетическую энергию частицы с абсолютной температурой в системе:
m*v2/2 = z/2*kB*T.
Где m - масса одной частицы, kB - Больцмана константа, v - скорость средняя квадратичная, z - число степеней свободы. Если обе части равенства умножить на количество N частиц в системе, то мы получим выражение для внутренней энергии U:
U = z/2*N*kB*T = z/2*n*R *T.
При записи этого выражения мы воспользовались следующими равенствами:
n = N/NA; R = kB*NA.
Теперь рассмотрим вопрос определения внутренней энергии газа с точки зрения термодинамики. Обратимся к изохорному процессу. В результате него все подводимое тепло идет на нагрев системы, поскольку объем остается постоянный, и работа газа равна нулю, то есть:
dU = Q.
В свою очередь, изменение величины U можно записать так:
dU = CV*dT.
Где CV - теплоемкость системы при постоянном объеме. Эта величина показывает, сколько энергии в джоулях необходимо затратить, чтобы нагреть систему на 1 Кельвин. Сравнивая это выражение с формулой для U, которая получена из кинетической теории, приходим к равенству:
CV = z/2*n*R.
Вместо теплоемкости CV часто пользуются молярной изохорной теплоемкостью, то есть той же величиной, только для 1 моля газа:
CV = z/2*R.
Формула Майера для теплоемкостей
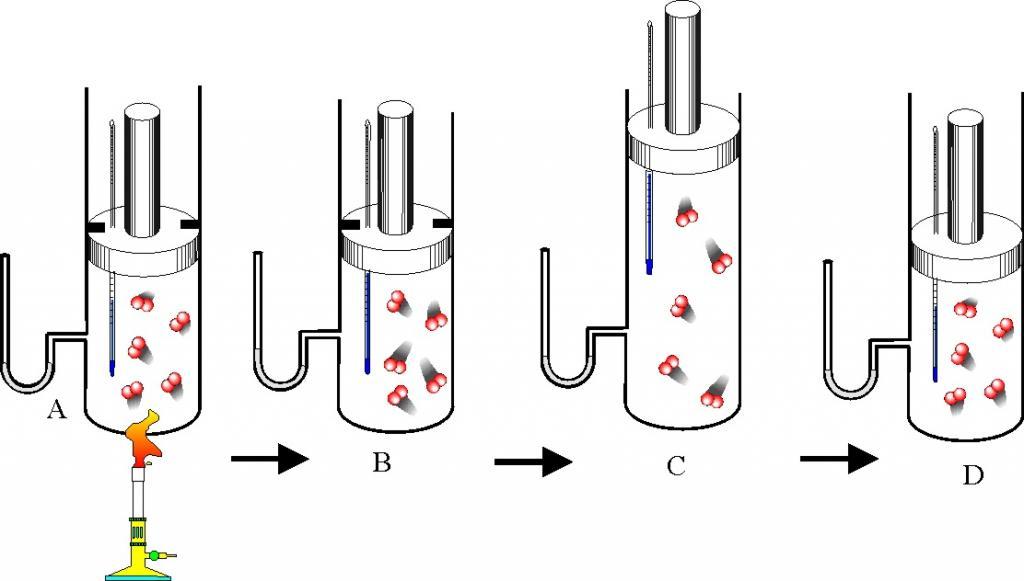
Чтобы получить названную формулу, следует рассмотреть с точки зрения термодинамики изобарный процесс. Под ним понимают переход системы между двумя равновесными состояниями, при котором давление не изменяется. Предположим, что в рассматриваемой системе содержится 1 моль газа, тогда первое начало термодинамики для изобарного процесса примет вид:
Q = dU + P*dV.
Теперь введем понятие об изобарной теплоемкости CP. Под ней понимают количество теплоты, которое следует системе сообщить, чтобы она нагрелась на 1 Кельвин, а ее давление при этом не изменилось. Это определение позволяет переписать равенство выше в виде:
CP*dT = dU + P*dV.
Если вспомнить уравнение для 1 моля идеального газа и выражение для изменения внутренней энергии, то это равенство запишется так:
CP*dT = CV*dT + R*dT =>
CP = CV + R.
Это выражение называется формулой Майера для идеального газа. Оно показывает, что изобарная теплоемкость всегда больше изохорной на величину газовой постоянной для 1 моля газа. Значение же газовой постоянной R также приобретает конкретный физический смысл - это работа, которую совершает один моль газа во время его изобарного расширения при нагреве на один Кельвин.
Задача на определение теплоемкостей воздуха
Необходимо вычислить молярные теплоемкости CP и CV для воздуха, полагая его идеальным газом.
Решить эту задачу несложно, если вспомнить, что изохорная молярная теплоемкость равна:
CV = z/2*R.
Тогда в соответствии с формулой Майера молярная величина CP будет равна:
CP = CV + R = (2+z)/2*R.
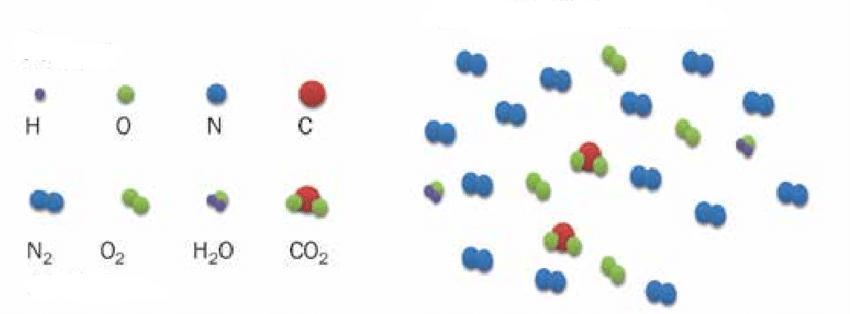
Поскольку воздух на 99% образован двухатомными молекулами O2 и N2, то z для него равно 5. Подставляя это значение, а также значение R=8,314 Дж/(К*моль) в формулы, получаем ответы на задачу: CV = 20,8 Дж/(К*моль), CP = 29,1 Дж/(К*моль).

