Бифторид аммония — токсичное неорганическое соединение промышленного производства, используемое в стекольной, нефтяной и металлургической сферах. Вещество часто применяется в качестве замены плавиковой кислоты или фтористого водорода.
Общее описание и физические свойства
Бифторид аммония чаще всего имеет твердое агрегатное состояние и представлено в виде кристаллов. Последние характеризуются высокой растворимостью в воде, но нулевой — в ацетоне и спирте. Кристаллы имеют орторомбическую сингонию с дискретной группой движений Р man. Вещество разлагается при температуре более 238 °С.
 Вам будет интересно:Ударение в слове "балованный": запомним благодаря буриме
Вам будет интересно:Ударение в слове "балованный": запомним благодаря буриме

Данный бифторид не обладает пожароопасными и взрывоопасными свойствами.
Структура и химическая формула
Вещество имеет несколько синонимичных наименований, таких как бифторид фторида аммония, аммоний фтористый кислый, гидрофторид аммония и т. д. Это соединение имеет химическую формулу NH4(HF2).
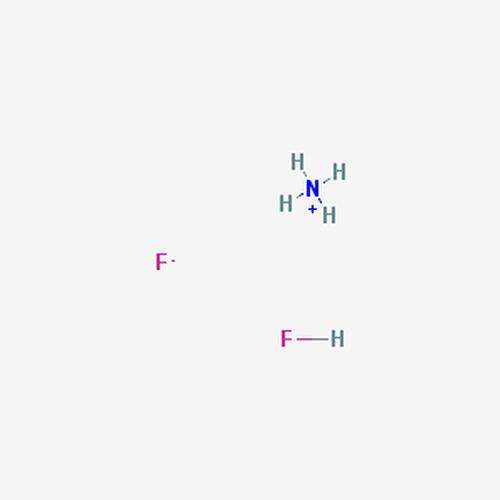
В химический состав вещества входят:
- катион аммония (NH4+);
- бифторид или водород дифторида;
- анион (HF2-).
Примечательной особенностью данного соединения является присутствие самой сильной водородной связи с длиной 114 мкм. Она соединяет фтор и водород в центросимметричном триатомном бифторидном анионе. Энергия этой связи превышает 155 кДж/моль-1.
В кристаллической форме вещества каждый катион аммония окружают четыре фторидных центра, образуя тетраэдр.
Форма производства
Бифторид аммония производится в двух формах:
- твердой (белые кристаллы);
- в виде раствора.

Раствор представляет собой прозрачную жидкость с запахом. Концентрация исходного вещества в такой смеси составляет от 28 до 30 %.
Использование вещества
Бифторид аммония имеет очень широкий спектр применения. В частности, его используют для:
- обработки стекла;
- анодирования алюминия;
- в качестве заменителя более токсичной и агрессивной плавиковой кислоты, что улучшает экологичность и снижает затраты стекольной обработки;
- очистки металлических поверхностей;
- дезинфицирования тепловых трубопроводов, изделий из кожи и дерева;
- литья марганца (в качестве флюса);
- удаления песка из нефтяных скважин;
- устранения ржавчины в котлах и трубах;
- промывки нефтяных проводов.
Замена плавиковой кислоты на гидрофторид аммония применяется не только в стекольной обработке, но и в бурении скважин.
Характеристика токсичности
Класс опасности бифторида аммония — АДР 8. Это достаточно токсичное для организма человека вещество с сильным коррозионным действием. При контакте с кожей это соединение вызывает раздражение, а при длительном воздействии — ожоги. Попадание бифторида аммония в глаза может вызвать повреждение зрительного органа.
Вдыхание кислорода в совокупности с этим веществом вызывает следующие симптомы:
- раздражение слизистых носоглотки и дыхательных путей;
- носовые кровотечения;
- кашель;
- хрипы;
- одышка;
- тошнота и рвота.
Взаимодействие бифторида аммония с водой приводит к образованию очень опасной фтористоводородной кислоты, что усиливает травмирующий эффект этого соединения при попадании на влажную кожу. В случае длительного и интенсивного воздействия вещества на организм его влияние приводит к отравлению фтором, боли в желудке, появлению слабости, судорог и даже смерти.
Регулярный контакт человека с бифторидом аммония приводит к развитию патологического состояния, называемого флюорозом, при котором происходит отложение фторидов в костях и зубах.
Экологичность
Для окружающей среды это вещество менее опасно, чем для человека при непосредственном контакте. Бифторид аммония обладает очень важным экологическим качеством — быстрым разложением (в течение нескольких дней), что исключает возможность его накопления.
Тем не менее во влажной среде это вещество распадается на фтороводородную кислоту и аммиак, которые токсичны для живых организмов.
