Реакции ионного обмена - это процессы, которые протекают между сложными веществами. Они должны сопровождаться появлением определенного результата: выпадением осадка, выделением газообразного соединения, образованием мало диссоциируемого вещества (например, воды).
Понятие о реакции
Курс органической химии рассматривает взаимодействия между соединениями, которые необходимы для жизнедеятельности человека и животных: белками, жирами, углеводами. Химическими принято называть такие процессы, которые протекают между веществами с получением иных соединений, отличающихся от исходных по свойствам и составу.
 Вам будет интересно:Как составлять план мероприятия? Составление плана проведения мероприятия: пример и структура
Вам будет интересно:Как составлять план мероприятия? Составление плана проведения мероприятия: пример и структура
Реакции ионного обмена - это типичный пример химических процессов, так как они сопровождаются изменением окраски, появлением газа, выпадением осадка.
Реагентами именуют исходные соединения, а продуктами – конечные соединения.
Движущей силой процесса является природа реагентов, особенности продуктов, концентрация реагирующих компонентов, температура, давление.
 Вам будет интересно:3 важнейшие войны 18 века: конфликты и итоги
Вам будет интересно:3 важнейшие войны 18 века: конфликты и итоги
Особенности взаимодействий
Реакции ионного обмена - это взаимодействие между веществами, взятыми в растворах. Как любые иные процессы химической природы, они протекают с выделением либо поглощением тепла, изменением окраски, агрегатного состояния.
В переводе с латинского языка «реакция» означает «ответное действие, отпор».
Именно поэтому реакции ионного обмена - это ответ одних веществ на атаку других.
Условия протекания
Среди тех факторов, которые необходимы для химического взаимодействия, выделяют:
- реагирующие соединения должны соприкасаться в максимальной степени;
- в некоторых случаях требуется повышение температуры;
- часть взаимодействий возможна только при воздействии электричества либо ультрафиолетового излучения.
Варианты классификации реакций
Сложно все процессы, сопровождающиеся изменением состава и свойств соединений, объединить в одну классификацию.
По возможности протекания процессов в прямом и обратном направлении неорганические и органические процессы делят на две группы.
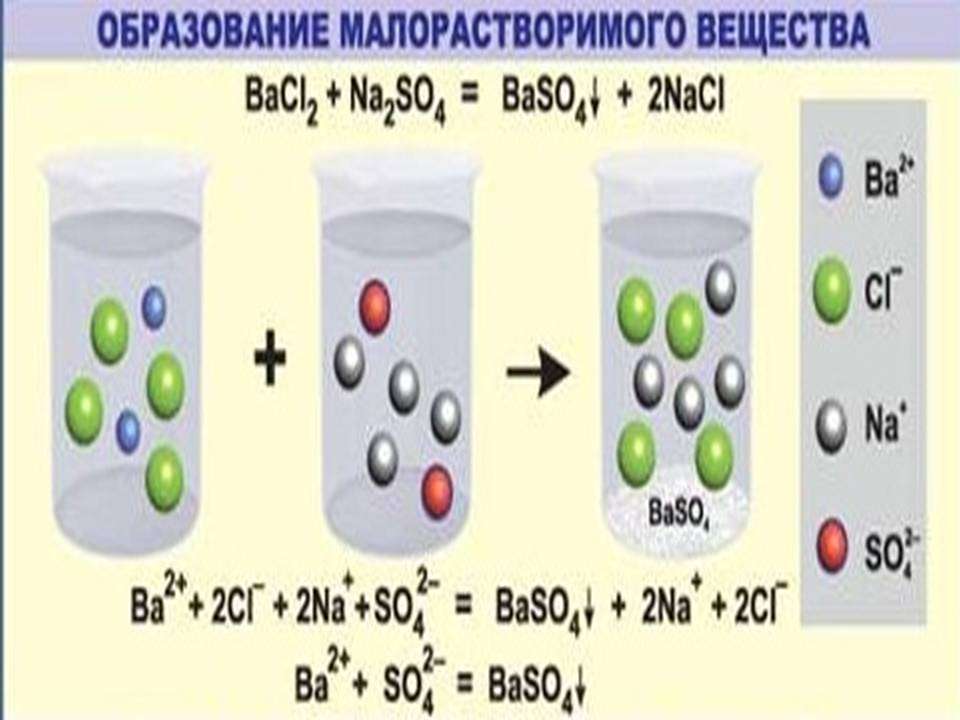
Необратимо протекает реакция ионного обмена между растворами растворимых соединений в том случае, когда между ними образуется нерастворимый продукт. Это применяется в аналитической химии для качественного определения катионов (анионов) в смеси растворов.
К примеру, для обнаружения катионов бария (Ba2+) используют раствор, содержащий сульфат анион (SO4 2-).
Пример ионных уравнений, сопровождающихся выпадением осадка

Как правильно составить уравнение процессов, характерных для этого случая? Рассмотрим на примере этой реакции ионного обмена сокращенные ионные уравнения. Данный вопрос входит в курс школьной программы, поэтому заслуживает пристального рассмотрения.
Первым этапом является написание процесса в молекулярном виде.
BaCl2+Na2SO4=BaSO4+2NaCl
Чтобы понять, действительно ли необратимо протекает реакция ионного обмена между растворами этих веществ, потребуется таблица растворимости кислот, солей, оснований. Одним из продуктов является сульфат бария (средняя соль), которая является нерастворимым соединением. Следовательно, процесс действительно необратим, сопровождается выпадением осадка.
Вторым этапом является запись полного ионного уравнения. Каждое из исходных соединений, продуктов взаимодействия записывается в виде катионов и анионов.
Ba2++ 2Cl-+2Na+ +SO42-=BaSO4+2Na+ + 2Cl-
В левой и правой частях данного уравнения положительные и отрицательные ионы, которые не связаны в осадок, малодиссоциируемое или газообразное соединение. После их сокращения получаем вариант краткого ионного уравнения.
Ba2++ SO42-=BaSO4
Пример процесса с образованием газа
Когда еще могут протекать реакции ионного обмена? Примеры с решением, предполагающим образование газообразного вещества, приведем для карбоната. Качественным реактивом на анион CO32- является взаимодействие с катионов водорода. Итогом процесса является образование углекислого газа.
Представим взаимодействие в молекулярном и ионном виде.
Na2CO3+2HCl=2NaCl+CO2+H2O
Продуктами реакции является углекислый газ и вода, которые не распадаются на ионы. Представим взаимодействие в полном ионном виде.
2Na++CO32-+2H++2Cl-=2Na++2Cl-+CO2+H2O
После сокращения ионов, повторяющихся в левой и правой частях, получаем следующий вид данного процесса:
CO32-+2H+=CO2+H2O
Получение малодиссоциируемого соединения
Какими еще признаками могут сопровождаться реакции ионного обмена? Примеры с решением приведем для классического процесса нейтрализации между раствором щелочи и кислоты.
Взаимодействие раствора соляной кислоты с гидроксидом натрия сопровождается образованием воды (малодиссоциируемого соединения). Проверить полноту протекания процесса можно с помощью индикатора. Если первоначально к щелочи добавить спиртовой раствор фенолфталеина, по мере добавления к нему соляной кислоты окраска будет исчезать (идет нейтрализация).
В молекулярном виде процесс выглядит следующим образом:
NaOH+ HCl=NaCl+H2O
Краткое ионное уравнение отражает процесс нейтрализации:
OH-+ H+=H2O
Заключение
В отличие от других разновидностей химических процессов, ионный обмен происходит только между растворами сложных соединений. Также среди обязательных условий, которые связаны с подобными процессами, отметим их необратимость. В тех случаях, когда среди продуктов есть малодиссоциируемое соединение, газообразное вещество, осадок, то можно говорить о полноте протекания процесса.
Если в случае замещения у соединений меняются степени окисления, то в случае ионного обмена валентное состояние атомов не меняется. Такие процессы протекают между сложными веществами: солями, кислотами, основаниями, оксидами.
Частным случаем таких взаимодействий является нейтрализация между щелочью и кислотой. Они подчиняются законам химического равновесия, идут в том направлении, где одно из соединений удаляют из реакционной сферы в летучем, газообразном виде, или как малодиссоциируемое вещество.
Химическая реакция является сложным процессом, который предполагает превращение одних веществ в другие, которые отличаются от исходных по строению, составу. Только при наличии одного из трех признаков, перечисленных выше, можно вести речь о полноте протекания взаимодействия.